|
Extraction d'espèces chimiques. Exercices |
|
|
Mots clés : Cours de chimie seconde Extraction, solvant, extraction par un solvant, hydrodistillation, distillation, Les différentes techniques d'extraction, extraction du diiode, QCM , extrcaton solide/liquide, extraction liquide/liquide, chlorophylle, chlorophylle brute, carotène, chromatographie, salade, épinards, chlorophylle a, chlorophyle b, spectre absorption , ... |
|
|
I-
Exercice 1 : Décrire des procédés d’extraction.
|
L’huile d’olive a
des propriétés bénéfiques sur le plan
cardio-vasculaire. Les huiles d’olives vierges sont obtenues à partir du fruit de l’olivier uniquement par des procédés mécaniques à froid
(lavage, malaxage,
pressage,
décantation
de
l’huile et de l’eau, centrifugation ou
filtration). Les huiles de grignons sont obtenues par traitement au solvant (heptane…) de grignons d’olive,
résidus composés
des fragments de peaux, de pulpe et
de noyaux.
Décrire les procédés
d’extraction cités en
gras
dans le
texte, en s’aidant éventuellement de
schémas. |
|
Pressage : Les olives sont nettoyées puis versées sur une piste de pierre sur laquelle tourne une lourde meule également de pierre, qui les broie, jusqu'à obtenir une pâte (Peau, pulpe et noyaux sont ainsi écrasés et broyés).
Cette pâte est déposée en couche sur des
couffins tressés, les
scourtins,
que l'on empile sous une presse, actionnée à la
main.
L'huile s'égoutte à
travers les mailles des scourtins entassés.
C’est la technique
de l’expression. Décantation : On laisse reposer le mélange huile-eau. L’huile et l’eau étant deux liquides non miscibles et l’huile étant moins dense que l’eau, elle surnage. On peut la récupérer grâce à une ampoule à décanter.
On peut aussi l’écoper avec un récipient adapté. Filtration : On laisse passer le mélange au travers d’un dispositif poreux pour séparer les phases liquides et solide du mélange.
Les scourtins retiennent la
partie solide constituée des restes de noyaux et de
pulpe d'olive et laissent s'écouler le liquide
composé d'huile et d'eau. Traitement au solvant : Les grignons d’olive sont mélangés à l’heptane qui extrait l’huile.
Car
l’huile est plus soluble dans l’heptane que dans l’eau.
On réalise une extraction par un solvant. |
II-
Exercice 2 : Choisir un procédé d’extraction.
|
La reine-des-prés contient, entre autres, de l’acide salicylique, principe actif efficace contre la fièvre et précurseur de l’aspirine. Cet acide est peu soluble dans l’eau froide, mais soluble dans l’eau chaude.
La notice d’une
boîte de tisane de reine-des-prés est reproduite
ci-dessous.
1)-
Quelle propriété de l’acide salicylique justifie
l’emploi de
la reine-des-prés comme tisane ?
2)-
L’utilise-t-on en décoction ou en infusion ?
Justifier. |
|
1)-
Propriété de l’acide salicylique :
- On utilise la
solubilité de l’acide salicylique dans l’eau chaude.
2)-
Il faut utiliser la tisane de reine-des-prés en
infusion, car ladécoction élimine l’acide
salicylique. |
III-
Exercice 4 : Décrire un procédé d’extraction.
|
L’urucum (ou roucou) est une plante d’Amazonie traditionnellementutilisée par des indiens pour se protéger du Soleil et des moustiques,
d’où le nom de « Peaux-Rouges »
qui leur était donné.
Les graines d’urucum
sont encore plus riches en bêta-carotène que
les
carottes.
La poudre qui en est
issue est insoluble dans l’eau, mais soluble dansl’éthanol ou les huiles végétales.
1)-
Proposer un solvant d’extraction possible à partir
des indications
du texte. Décrire le procédé à
mettre en œuvre.
2)-
Un livre indique la recette suivante :
- « Laisser
l’urucum au contact de l’huile végétale pendant 5
jours, en remuant de temps en temps. Filtrer.
On
peut aussi laisser se faire naturellement la
séparation. »
- Nommer les trois
techniques évoquées dans cette recette. |
|
1)- Comme solvant d’extraction, on peut utiliser l’éthanol.
Il est dit dans l’énoncé que la poudre
d’urucum est soluble
dans l’éthanol.
2)-
Les techniques évoquées : ► « Laisser l’urucum au contact de l’huile végétale pendant
5 jours, en
remuant de temps en temps » :
-
Extraction par un
solvant.
►
« Filtrer »
-
La filtration.
►
« On peut aussi
laisser se faire naturellement la séparation. »
-
La décantation. |
IV-
Exercice 6 : Séparer les phases de l’hydrodistillat.
|
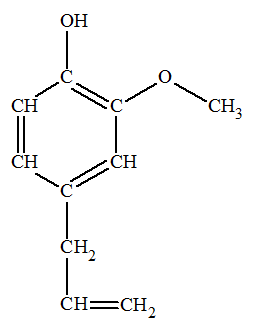
L’eugénol, aux
effets antiseptiques, entre dans la composition de
nombreux médicaments (solutions pour usage
dentaire).
Elle est obtenue par
hydrodistillation des clous de girofle.
Une extraction par
un solvant est nécessaire pour récupérer
l’huile
essentielle présente dans le distillat.
On assimilera
l’huile essentielle à l’eugénol.
L’eugénol est peu
soluble dans l’eau et insoluble dans l’eau salée.
Il est cependant
très soluble dans l’éthanol, le dichlorométhane,
et
un peu dans le chloroforme.
L’éthanol est
miscible à l’eau.
Le dichlorométhane
et le chloroforme sont non miscibles à l’eau.
1)-
Quel solvant d’extraction peut-on à priori choisir ?
Justifier. 2)- Lors de l’extraction, une étape consiste à ajouter du chlorure de sodium dans la phase aqueuse :
Quel
est l’intérêt de cette technique ? |
|
1)-
Comme solvant on peut choisir le dichlorométhane :
-
L’eugénol est plus
soluble dans le dichlorométhane que dans l’eau,
- Et le
dichlorométhane est insoluble dans l’eau.
- Remarque 1 : on ne
choisit pas le chloroforme car l’eugénol est plus
soluble dans le dichlorométhane que dans le
chloroforme.
- Remarque 2 : on ne
choisit pas l’éthanol bien que l’eugénol y soit très soluble car l’éthanol est miscible à
l’eau.
2)-
L’ajout de chlorure de sodium à l’eau s’appelle
le
relargage.
- Cette technique
permet d’éliminer l’eugénol encore présent dans la
phase aqueuse et de la faire passer dans la phase
organique (dichlorométhane)
Eugénol :
2-methoxy-4-(prop-2-en-1-yl)phenol
Formule brute : C10H12O2
|
V-
Exercice 9 : L’estragol.
|
L’estragol est une espèce chimique présente dans les feuilles d’estragon. L’huile essentielle d’estragon aurait des vertus antiallergiques.
Elle peut être
extraite par hydrodistillation.
Les phases aqueuse
et organique de l’hydrodistillat obtenu
sont très
difficiles à séparer par une simple décantation.
1)- Parmi les solvants proposés dans le tableau ci-dessous,
lesquels peut-on à priori choisir ?
Justifier la réponse.
2)-
Pour des questions de santé et de sécurité, l’un de
ces solvants
est à éviter particulièrement :
lequel ?
3)-
Décrire les différentes opérations à effectuer lors
de cette
extraction par un solvant.
4)-
Schématiser ces différentes étapes, en précisant les
positions
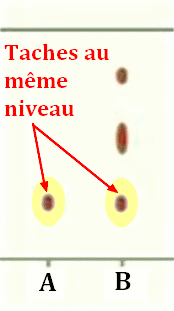
des phases. 5)- Pour vérifier la présence d’estragol dans l’extrait obtenu, on réalise une chromatographie. Le chromatogramme obtenu est représenté ci-dessus. Les lettres correspondent aux dépôts d’estragol pur (en A) et d’extrait (en B).
Interpréter le
chromatogramme.
|
|||||||||||||||||||||||||||||||||||||||||||||
|
1)-
Choix du solvant :
- On peut utiliser le
cyclohexane et le dichlorométhane.
- Ils sont non
miscibles à l’eau et l’estragol y est soluble.
- Remarque :
on ne choisit pas l’éthanol bien que l’estragol y
soit soluble car l’éthanol est miscible à
l’eau.
2)-
Questions de santé et de sécurité :
-
Le dichlorométhane
est suspecté d’être cancérogène, il faut éviter de
l’utiliser.
3)-
Différentes opérations à effectuer lors de cette
extraction
par un solvant :
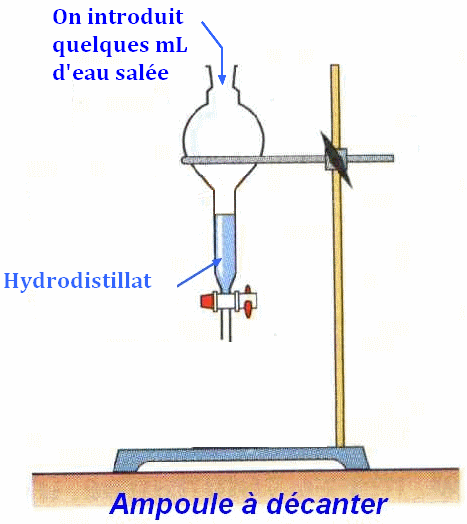
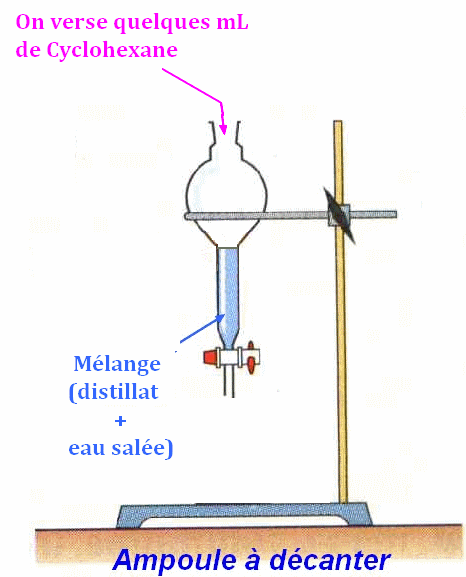
- Introduire
l’hydrodistillat dans une ampoule à décanter.
-
Introduire de l’eau
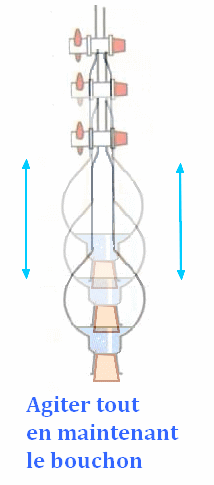
salée, fermer et secouer pour effectuer un lavage. - Introduire quelques mL de cyclohexane, boucher l’ampoule
à décanter,
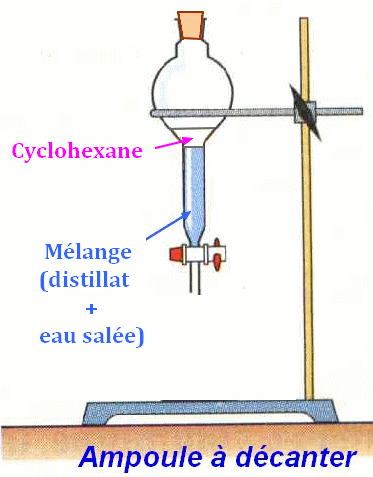
agiter et laisser décanter.
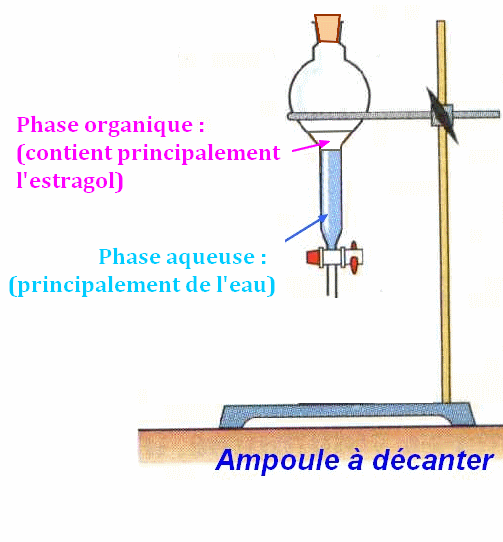
-
Récupérer la phase
organique (phase supérieure).
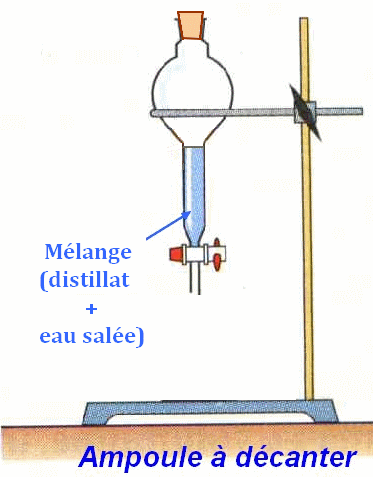
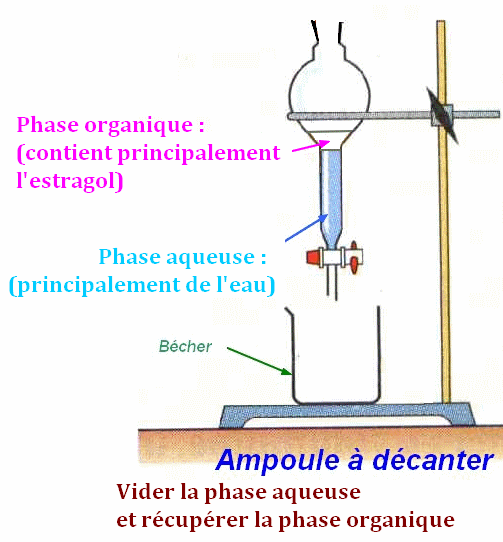
4)-
Schémas de l’extraction par un solvant.
Ne pas oublier de
mettre le bouchon et de le maintenir
On laisse reposer le
mélange
On laisse décanter
5)-
Interprétation du chromatogramme :
-
L’extrait est un
mélange (plusieurs taches) qui contient de
l’estragol (deux taches au même niveau)
|
VI-
Exercice 10 : Dangereux solvant.
|
Pendant très
longtemps le café a été décaféiné par
extraction de
la caféine à l’aide du trichlorométhane
(chloroforme) dont un extrait de l’étiquette est
fourni ci-après :
1)-
Quel est l’état physique du trichlorométhane à 25 °
C.
2)-
La caféine est-elle soluble dans le
trichlorométhane ?
3)-
Pour quelle raison a-t-on abandonné l’extraction de
la caféine par le trichlorométhane ?
4)-
On dispose, au laboratoire, d’une préparation à base
de café qui contient entre autres, de la caféine
dissoute
dans l’eau. - Sachant que la caféine est peu soluble dans l’eau, proposer un protocole opératoire permettant d’extraire la caféine de cette préparation.
Faire un schéma illustrant l’étape principale de l’extraction en
précisant la position des diverses phases. |
|
1)-
À 25 ° C, le trichlorométhane se trouve à l’état
liquide :
2)-
La caféine est soluble dans le trichlorométhane car
c’est le solvant utilisé pour l’extraire.
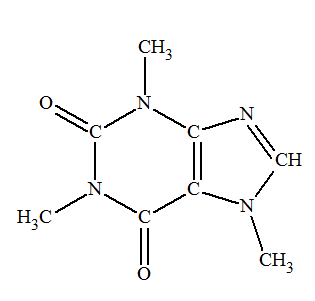
La caféine :
C8H10N4O2
3)-
Le trichlorométhane :
Pictogrammes harmonisés
-
Le trichlorométhane
est toxique
- H302 : Nocif en cas d'ingestion ; H315:
Provoque une irritation cutanée
- H351 : Susceptible
de provoquer le cancer.
- H373 : Risque
présumé d'effets graves pour les organes à la suite
d'expositions répétées ou d'une exposition
prolongée.
- Autant éviter de
l’utiliser.
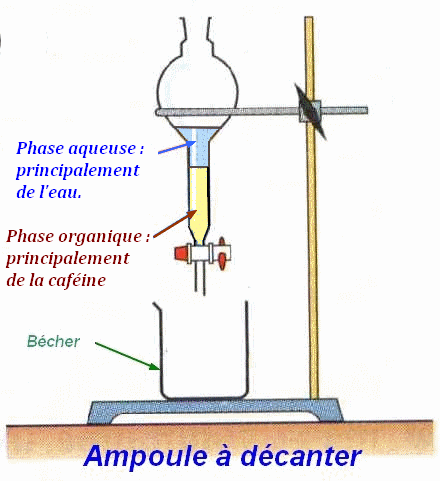
4)-
Protocole opératoire de l’extraction par
un
solvant :
- On ajoute du
trichlorométhane à la solution aqueuse de caféine
dans une ampoule à décanter.
- On agite et on
laisse décanter :
- La phase organique
plus dense que la phase aqueuse se situe en dessous.
-
On recueille la
phase organique qui contient principalement la
caféine. |
VII-
Exercice 15 : Les bienfaits de la menthe poivrée.
|
La menthe poivrée a
des propriétés anti-inflammatoires et antivirales,
dues entre autres au menthol et à l’eucalyptol.
On la trouve
traditionnellement dans les pastilles contre
le mal
de gorge.
L’huile essentielle
est obtenue par hydrodistillation des
feuilles de
menthe poivrée.
1)-
Schématiser et légender le montage.
On cherche à
déterminer la composition de l’huile
essentielle de
menthe poivrée.
On réalise pour cela une
chromatographie sur couche
mince avec un éluant
adapté.
Le chromatogramme est donné ci-après.
2)-
Quel est le rôle de l’éluant ?
3)-
Que représentent les traits situés en haut et en
bas
du chromatogramme ?
4)-
Interpréter le chromatogramme obtenu. |
|
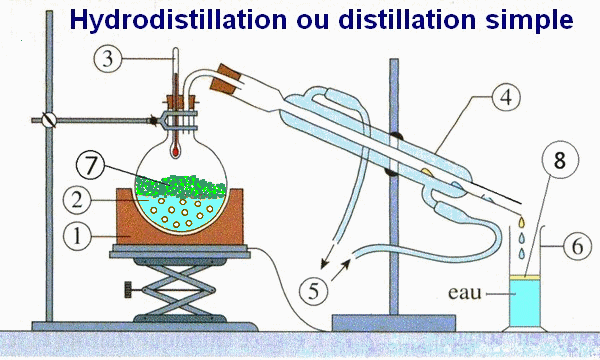
1)-
Schéma légendé du montage d’hydrodistillation.
- Légende :
1 : Vallet (support)
2 : Mélange
(Eau-feuille de menthe poivrée)
3 : Thermomètre
4 : Réfrigérant à
eau
5 : Arrivée et
Sortie de l’eau
6 : Éprouvette
7 : Feuilles de
menthe poivrée broyées.
2)-
Rôle de l’éluant : Il permet de solubiliser
les
espèces chimiques et de les faire migrer
sur le
support.
3)-
Les deux traits :
- Trait le plus bas :
la ligne de dépôt des espèces chimiques
- Trait supérieur :
front de l’éluant.
4)-
Interprétation du chromatogramme :
- Du chromatogramme,
on peut déduire que la menthe poivrée contient du
menthol, de l’eugénol et d’autres espèces chimiques
inconnues.
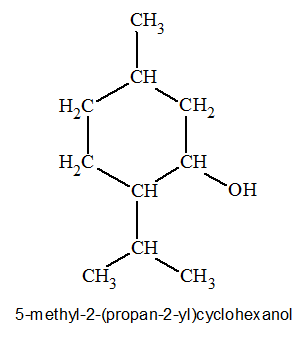
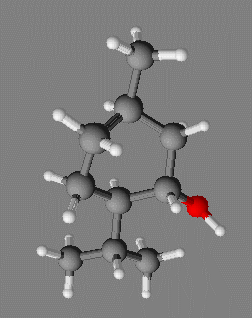
Le menthol :
C10H20O
|
VIII-
Exercice 17 : L’huile de palme.
|
À cause de son faible coût, l’huile de palme est massivement utilisée dans une grande variété de produits alimentaires.
La demande croissante a un impact
majeur en termes
d’écologie et de sécurité
alimentaire : ► Les plantations de palmiers à huile entraînent une déforestation intensive de l’Asie du Sud-est (essentiellement l’Indonésie et la Malaisie) et augmentent significativement
l’effet de
serre : ► L’huile de palme est composée d’acides gras trans dont la consommation est nuisible pour la santé. D’après l’AFSSAPS (Agence française de sécurité sanitaire des produits de santé) et l’EFSA (Autorité européenne de Sécurité des aliments),
ils doubleraient le risque d’accident
cardiovasculaire.
L’huile de palme est
néanmoins un ingrédient essentiel de
la cuisine
africaine, car elle est extraite de la pulpe des
fruits
du palmier à huile,
arbre
endémique
de certaines régions
tropicales (Tanzanie, Bénin,
Nigéria, Sénégal, Togo)
Les méthodes
d’extraction artisanales de l’huile de palme
varient, mais on retrouve toujours les mêmes grandes
étapes :
►
Égrappage,
puis ébouillantage des fruits ; ► Malaxage : les fruits sont déchiquetés et l’huile est libérée. De l’eau bouillante est apportée au malaxeur artisanal.
L’huile est entraînée par l’eau et le mélange
eau-huile s’écoule dans un bassin de réception ;
►
L’huile qui flotte
au-dessus de l’eau, peut en être aisément séparée.
L’addition de sel facilite le processus ;
►
L’huile est
écopée à la
calebasse et filtrée au travers d’un tamis qui
retient les quelques fibres entraînées.
1)-
Rechercher la signification des mots et expression
en gras dans le texte.
2)-
Dans quels produits alimentaires d’usage courant
trouve-t-on de l’huile de palme ? (consulter les
étiquettes dans les lieux de vente)
3)-
Pourquoi n’est-il ni écologique ni sain de consommer
de l’huile de palme ?
4)-
Nommer les différents procédés d’extraction et de
séparation cités dans le texte.
5)-
La densité de l’huile est-elle plus grande ou plus
petite que celle de l’eau ?
6)-
L’huile est insoluble dans l’eau salée. À quoi sert
l’addition de sel ?
7)-
Extraction de l’huile de palme :
a)-
La température de
fusion de l’huile de palme est comprise entre 36 ° C
et 40 ° C. Quel est l’état physique de l’huile de
palme à 25 ° C
b)-
Pourquoi
l’extraction se fait-elle à chaud ? |
|
1)-
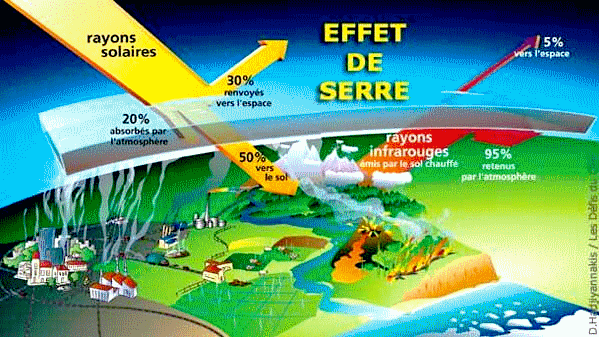
Mots et expressions : - Effet de serre : C’est un processus naturel qui, pour une absorption donnée d'énergie électromagnétique, provenant du Soleil (dans le cas des corps du système solaire) ou d'autresétoiles (dans le cas général),
confère au
corps qui reçoit cette énergie une température de
surface nettement supérieure à une situation « sans
effet de serre ». - « L'effet de serre » est dû à la présence de gaz à effet de serre (GES) contenus dans l'atmosphère. - Une partie du rayonnement solaire traverse l'atmosphère et atteint le sol, qui en retour émet un rayonnement thermique qui, lui, est absorbé par les GES, ce qui réchauffe l'atmosphère, qui elle-même réchauffe le sol (dans le cas de la Terre : la croûte terrestre, la biosphère et l'hydrosphère).
- Une augmentation de la
concentration des gaz à effet de serre dans
l'atmosphère participe au réchauffement climatique.
- Endémique : une espèce est dite endémique d'une région déterminée si elle n'existe que là. Une espèce endémique (ou un taxon endémique) l'est obligatoirement par rapport à un territoire nommé :
le koala est
endémique de l'Australie,
le cyprès de Lambert est
un arbre endémique de la
Californie (même s'il a
ensuite été planté dans le
monde entier).
-
Égrappage :
les
fruits du palmier
sont
séparés de la rafle du régime.
huile de palme - Écopée à la calebasse : La crème huileuse qui flotte en surface est récupérer grâce à un récipient plat, la calebasse fruit du calebassier dont l'arbre est originaire d'Amérique tropicale et a été introduit dans tous les pays tropicaux.
La calebasse est appelée
COUI
dans les caraïbes et
elle est utilisée comme
récipient par les ménagères dans
leur cuisine et
comme écope par les pêcheurs.
2)- Produits alimentaires d’usage courant contenant
de
l’huile de palme :
-
Elle est présente
quasiment à notre insu dans la plupart des produits
que nous consommons au quotidien.
- L’huile de palme est
mentionnée sur les étiquettes, parfois avec la
simple mention "huile végétale" dans l'alimentation.
- La mention "huile
végétale" renferme : huile de colza et huile de
palme le plus souvent.
- Lorsque le produit
ne contient que de l’huile de colza, cela est
indiqué sur l’étiquette.
- Si le produit
contient de l’huile de palme et de l’huile de colza,
alors sur l’étiquette du produit, il y a la
mention : "huile végétale".
3)-
Les dangers de l’huile de palme : - Les plantations de palmiers à huile entraînent une déforestation intensive.
- L’huile de palme est composée d’acides
gras trans dont la consommation est nuisible pour la
santé.
- Cette huile
massivement utilisée par l'industrie
agro-alimentaire est aussi fortement suspectée de
favoriser les troubles cardio-vasculaires chez les
populations occidentales.
- L'huile de palme est
aujourd'hui la plus consommée dans le monde (25 %),
dépassant de peu l'huile de soja (24 %) et de loin
celles de colza (12 %) et de tournesol (7 %).
4)-
Les différents procédés d’extraction et de
séparation
cités dans le texte :
►
Texte 1: Malaxage :
les fruits sont déchiquetés et l’huile est libérée
-
Procédé 1:
l’expression.
►
Texte 2 : L’addition
de sel facilite le processus
-
Procédé 2 : le
relargage.
►
Texte 3 : L’huile
est écopée à
la calebasse :
-
Procédé 3 : la
séparation.
►
Texte 4 : filtrée au
travers d’un tamis qui retient les quelques fibres
entraînées ;
- Procédé 4 : la
filtration.
5)-
Densité de l’huile de palme :
-
L’huile de palme,
qui surnage sur la phase aqueuse car elle peut être
écopée à la calebasse, a une densité inférieure à
celle de l’eau.
6)-
Addition de
sel : le relargage.
- L’extraction de
l’huile de palme est facilitée
par l’ajout de sel car l’huile est moins
soluble dans l’eau salée que dans l’eau.
7)-
Extraction de l'huile de palme :
a)-
À 25 ° C, l’huile de
palme se trouve à l’état solide.
b)-
L’extraction se fait
à chaud afin que l’huile de palme se trouve à l’état
liquide. |
|
|